Рандомизированное контролируемое исследование в медицине
Рандомизированные контролируемые исследования являются золотым стандартом получения научных данных о новых медицинских вмешательствах.
Это означает, что выпуская новый лекарственный препарат, новый метод диагностики или лечения, компания-производитель должна проверить как эффективность, так и безопасность своего метода исследования или лечения, проведя рандомизированное контролируемое исследование (РКИ).
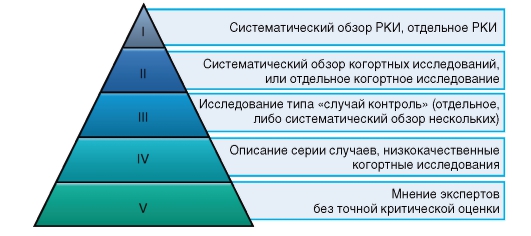
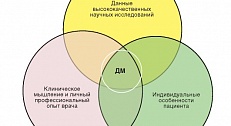
На схеме показана т.н. пирамида доказательности. Как видите РКИ занимает первое место в этой иерархической системе.
Это означает, что выпуская новый лекарственный препарат, новый метод диагностики или лечения, компания-производитель должна проверить как эффективность, так и безопасность своего метода исследования или лечения, проведя рандомизированное контролируемое исследование (РКИ).

На схеме показана т.н. пирамида доказательности. Как видите РКИ занимает первое место в этой иерархической системе.
Что же означают эти три слова в данном методе клинического анализа: рандомизированное контролируемое исследование?
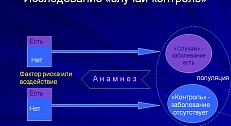
Рандомизированное – означает, что решение о том, в какую группу попадет пациент, в испытательную (ту, в которой будут испытывать новый метод), традиционную (ту, в которой будет использоваться общепринятое лечение данного заболевания) или в контрольную (ту, в которой будут использовать плацебо, то есть «пустышку») принимается совершенно случайным образом.
Контролируемое – означает, что в исследовании обязательно будет осуществляться контроль, путем сравнения с традиционным методом лечения, или с группой плацебо.
Исследование – напоминает, что препарат проходит испытание, в ходе которого он обязан показать как свою эффективность в лечении этой патологии, так и свою безопасность, в противном случае ему никогда не попасть в аптеки.
Рандомизированное – означает, что решение о том, в какую группу попадет пациент, в испытательную (ту, в которой будут испытывать новый метод), традиционную (ту, в которой будет использоваться общепринятое лечение данного заболевания) или в контрольную (ту, в которой будут использовать плацебо, то есть «пустышку») принимается совершенно случайным образом.
Контролируемое – означает, что в исследовании обязательно будет осуществляться контроль, путем сравнения с традиционным методом лечения, или с группой плацебо.
Исследование – напоминает, что препарат проходит испытание, в ходе которого он обязан показать как свою эффективность в лечении этой патологии, так и свою безопасность, в противном случае ему никогда не попасть в аптеки.
Почему в клинических исследованиях требуется рандомизация?
Случайный отбор кандидатов крайне важен, поскольку в противном случае, если мы предоставим пациенту или врачу выбирать, в какую группу поместить участника исследования, это может сильно исказить полученные результаты.
Благодаря рандомизации мы избавляемся от всякой предвзятости и делаем группы максимально однородными: по полу, возрасту, анамнезу, длительности заболевания, осложнениям, сопутствующим заболеваниям и т.д., чтобы сократить количество искажений результатов исследования от посторонних факторов до минимума.
Скажем, если врач очень хочет получить положительные результаты от изобретенного им препарата, он может сознательно или неосознанно помещать более тяжелых пациентов в группу плацебо (т.е. в группу контроля), а менее тяжелых пациентов – в группу, получающую экспериментальный препарат. Тогда он гарантированно получит в экспериментальной группе лучшие показатели лечения, но таким показателям совсем нельзя будет доверять.
А теперь представьте себе, что врач не просто хотел бы получить хорошие результаты, но и подкуплен фармацевтической компанией, напрямую заинтересованной в самых положительных результатах исследования их нового препарата. В таком случае ставки очень высоки, и финансовые потоки – тоже. Именно поэтому, проводя тщательную рандомизацию пациентов, мы исключаем не только любую предвзятость, но и любое случайное искажение.
К СВЕДЕНИЮ: Еще одним методом объективизации данных, полученных в РКИ является ослепление. Слепой метод, или ослепление - это метод проведения исследования, заключающийся в сокрытии информации от того или иного участника исследования, призванный исключить субъективное воздействие участников исследования на результат. Если РКИ сопровождалось ослеплением, то в таком случае говорят о [двойном] слепом рандомизированном клиническом исследовании. Подробнее об ослеплении (слепом методе исследования): СЛЕПОЕ ИССЛЕДОВАНИЕ
Зачем клинические испытания «контролируются»?
Это важно для того, чтобы четко понимать, какие преимущества (или риски) напрямую связаны с действием препарата, а какие являются следствием болезни, других препаратов, применяемых одновременно с исследуемым, или посторонних факторов.
«После того – не значит вследствие того» - говорили еще древние римляне. Если не проводить сравнение с группами контроля, то можно получить выраженный положительный или выраженный негативный эффект, не имеющий ничего общего с исследуемым препаратом, и ошибочно утвердиться в мысли, что между приемом препарата и этим эффектом есть прямая причинно-следственная связь.
Еще одним обязательным свойством исследования, увеличивающим степень контроля, является наличие достаточно большого количества участников исследования. Это необходимо, чтобы случайные различия и необычные случаи не оказывали большого влияния на полученные результаты.
Контрольная группа обычно получает плацебо: это препарат-пустышка, который выглядит, пахнет, имеет вкус идентичный настоящему препарату, однако не содержит действующего вещества.
ЭФФЕКТ ПЛАЦЕБО (PLACEBO EFFECT) — как правило (но не обязательно или не всегда), благоприятный эффект, приписываемый пациентами лекарственному средству или лечению, назначенному лечащим врачом. Ощущаемое благоприятное действие плацебо связано с ожиданием эффекта от лечения, например, из-за внушения. Подробнее об эффекте плацебо.
Сравнение со стандартным лечением
Помимо группы плацебо, сравнение нередко происходит с группой, получавшей стандартное и общепринятое при изучаемой патологии, лечение. Целью такого сравнения является определить, каковы преимущества и каковы риски экспериментальной терапии по сравнению со стандартной.
Тот факт, что новый препарат оказывает терапевтический эффект при данном заболевании – недостаточен для его одобрения и широкого использования. Он должен быть более эффективен и/или более безопасен, нежели стандартная общепринятая терапия, хотя бы в некоторых случаях, при определенных известных условиях.
Кроме всего этого, немаловажным является стоимость новой терапии, в сравнении со стоимостью стандартного лечения. Если препарат менее эффективен, но значительно более дешев – это может стать аргументом в его пользу.
Непрактичность и неэтичность плацебо в некоторых РКИ
Строгий научный дизайн исследования - не всегда является практичным. Бывает весьма сложно имитировать лечение в группе плацебо, чтобы пациент не мог определить, в какой он группе. Кроме того, существуют ситуации, когда терапия плацебо является неэтичной. Поэтому проведение РКИ может стать невозможным в следующих случаях:
- Многие агрессивные или инвазивные процедуры (с применением специального медицинского аппарата, или с применением хирургической операции) невозможно, или неэтично имитировать. Нельзя разрезать человеку ткани, только чтобы он не догадался, где находится, в лечебной, или в контрольной группах.
- Заболевание может быть слишком редким, и у ученых нет возможности набрать такое количество пациентов, которое обеспечит достоверность полученных научных данных.
- Подбор пациентов к конкретному исследованию может быть слишком трудным.
Нередко плацебо-контроль просто невозможен, поскольку промедление с лечением может нанести непоправимый ущерб организму пациента, или даже привести к его гибели. В таком случае совершенно недопустимо отказывать пациенту в стандартном лечении, какая бы высокая научная цель не стояла за таким экспериментом.
Если подобные препятствия не позволяют провести РКИ, то для такого исследования выбирается иной, более подходящий дизайн. Решение о допустимости проведения РКИ принимается специальным этическим комитетом. Клиническое испытание не может быть начато без одобрения этого комитета