Внутрисуставные инъекции. Что нужно знать врачу?
Аннотация
В течение нескольких десятилетий внутрисуставные инъекции кортикостероидов используются при лечении симптоматического остеоартрита коленного сустава и в настоящее время остаются частой практикой.
Считается, что обезболивающий эффект от инъекции стероида обусловлен уменьшением воспаления в пораженном артритом коленном суставе. Медицинские работники по-разному выполняют эту процедуру, включая различия в месте инъекции, используемых лекарственных препаратах и уровне стерильности. Успех инъекций стероидов для облегчения боли в коленном суставе при артрите чаще всего быстро достигается.
Тем не менее, в опубликованной литературе эффективность внутрисуставных инъекций кортикостероидов различается. Последнее клиническое руководство Американской академии хирургов-ортопедов (American Academy of Orthopaedic Surgeons) не поддерживает убедительные рекомендации по применению внутрисуставных инъекций кортикостероидов для лечения симптоматического остеоартрита коленного сустава.
Медицинские работники должны знать о нежелательных эффектах и потенциальных осложнениях этих инъекций при использовании их в клинической практике.
Введение
Остеоартрит является основной причиной нетрудоспособности у взрослых и поражает, согласно оценкам, 52,5 миллионов взрослых в Америке. [1] Коленный сустав - одна из наиболее частых локализаций этого заболевания, и поражение колена оказывает самое большое влияние на трудоспособность; на его долю приходится 83% общего бремени нетрудоспособности остеоартрита. [2]
Распространенность остеоартрита в современную постиндустриальную эпоху удвоилась. [3] Способы излечения остеоартрита пока неизвестны. Стандартные методы лечения, включая внутрисуставные инъекции стероидов, направлены на облегчение симптомов. Внутрисуставные инъекции стероидов, как полагают, оказывают эффект за счет уменьшения воспаления в суставе и синовиальной оболочке, хотя точный механизм не известен. [4–6] Показания к их применению включают кратковременное симптоматическое облегчение остеоартроза после неэффективности других терапевтических мер.
Международная группа Общества по изучению остеоартрита (Osteoarthritis Research Society International group) в 2014 году опубликовала обновленные, основанные на научных данных, консенсусные рекомендации по лечению остеоартрита коленного сустава, в которых указано, что внутрисуставные инъекции стероидов подходят для пациентов с остеоартритом коленного сустава и полиартритом, с сопутствующими заболеваниями или без сопутствующих заболеваний для кратковременного облегчения боли. [7].
С другой стороны, Американская академия хирургов-ортопедов не смогла поддержать убедительные рекомендации относительно применения внутрисуставных кортикостероидов в пациентов с симптоматическим остеоартритом коленного сустава [8]. Рабочая группа обнаружила ограниченные высококачественные клинические данные только в четырех сравнительных исследованиях с плацебо, соответствующих их критериям, а результаты оказались противоречивыми. [8]
Хотя убедительные данные отсутствуют, внутрисуставные инъекции кортикостероидов для лечения остеоартрита коленного сустава продолжают часто использоваться.
Тип кортикостероида для внутрисуставных инъекций
Выпускаются различные кортикостероиды для внутрисуставных инъекций [4,9–13] (Таблица 1). Однако клинические данные, сравнивающие различные инъекционные стероиды, ограничены. В 2009 году Hepper et al [14] провели систематический обзор и обнаружили четыре исследования I уровня, в которых сравнивались три разных кортикостероида: бетаметазон, метилпреднизолон и триамцинолон. Их анализ показал, что триамцинолон более эффективен, хотя не все показатели были валидированы, а методика последующего наблюдения и дозы стероидов не были стандартизированы между исследованиями.
Таблица 1. Часто используемые инъекционные кортикостероиды, их концентрации и дозировка
|
|
Инъекционные кортикостероиды
|
Концентрация (мг/мл)
|
Обычная доза для крупного сустава (мг)
|
|
Бетаметазон (часто смесь бетаметазона ацетата и бетаметазона натрия фосфата)
|
6
|
6–12
|
|
Метилпреднизолона ацетат
|
20, 40 или 80
|
20–80
|
|
Триамцинолона ацетонид
|
10 или 40
|
10–40
|
|
Триамцинолона диацетат
|
40
|
20–40
|
|
Триамцинолон гексацетонид
|
20
|
10–20
|
|
Дексаметазона натрия фосфат
|
4 или 8
|
2–4
|
Триамцинолон гексацетонид может быть более эффективным благодаря плохой растворимости, что обеспечивает более длительное поддержание уровня лекарственного средства в суставе и синовиальной оболочке и более низкие системные уровни по сравнению с соединениями, которые лучше растворяются. [15]
Опрос врачей-членов Американской коллегии ревматологов (American College of Rheumatology), посвященный использованию инъекционных кортикостероидов при лечении коленного сустава, показал, что 34,6% врачей использовали метилпреднизолона ацетат, 31,2% применяли триамцинолона гексацетонид, и 21,7% использовали триамцинолона ацетонид, тогда как остальные врачи применяли для инъекций другие стероиды.
Наиболее частой причиной использования метилпреднизолона ацетата (71,9%) и триамцинолона ацетонида (51,9%) была «доступность» или «привычка», тогда как самой частой причиной применения триамцинолона гексацетонида (76,3%) была «эффективность» или «более длительное действие». [16] Однако идея о том, что триамцинолона гексацетонид может быть более эффективным, не поддерживается убедительными данными и даже противоречит недавнему рандомизированному двойному слепому исследованию, сравнивающему инъекции триамцинолона гексацетонида и метилпреднизолона ацетата при остеоартрите коленного сустава, в котором обнаружено, что оба препарата одинаково эффективны для уменьшения боли в течение 24 недель во все моменты времени (P = 0,523). [17] Поэтому еще предстоит определить, какой стероид самый лучший.
Стремление добиться более длительного сохранения внутрисуставных уровней стероидов с более медленным и сниженным системным поглощением привело к появлению новых лекарственных форм стероидов. Bodick et al [18] провели двойное слепое рандомизированное клиническое исследование 2 фазы для изучения лекарственной формы триамцинолона ацетонида с пролонгированным высвобождением (FX006) по сравнению с обычной лекарственной формой с немедленным высвобождением.
Результаты показали, что доза FX006 40 мг обеспечивала лучшее обезболивание по сравнению с триамцинолоном немедленного высвобождения в дозе 40 мг в течение 2–12 недель со статистически значимым преимуществом в каждый момент времени между 5 и 10 неделями после инъекции (P <0,05). [18] Нежелательные явления были легкими и сопоставимыми между всеми группами. Устойчивые местные эффекты этого лекарственного препарата с безопасным профилем перспективны для будущего использования.
Доза кортикостероидов
Разнообразие типов кортикостероидов усугубляется разнообразием используемых доз стероидов. Клинические данные в отношении различных доз каждого кортикостероида ограничены. Рекомендуемая доза кортикостероида зависит от фармакологической активности и растворимости препарата. Дозировка стероида и объем введения определяются мнением врача и имеющимися в продаже препаратами. Общее правило для применения лекарств в целом – использовать наименьшую возможную дозу для достижения желаемого результата. Данные, поддерживающие использование доз, превышающих рекомендованные производителем, для каждого соединения минимальны. [11]
Сочетание с местными анестетиками
Медицинские работники часто комбинируют местный анестетик с внутрисуставным кортикостероидом перед инъекцией. [16] Причины использования местного анестетика включают немедленное облегчение боли при внутрисуставной патологии (т. е. диагностические и терапевтические эффекты), разведение стероида и уменьшение или устранение послеинъекционного обострения. Немедленное облегчение боли после внутрисуставного введения местного анестетика может помочь в диагностировании основной причины боли пациента, если она является многофакторной.
Нередко у пациентов с остеоартритом коленного сустава есть и другие источники боли вокруг коленного сустава (например, бурсит, тендинит и неврит, особенно неврит подкожного нерва), которые иногда ошибочно связывают с болью при остеоартрите. Если боли в значительной степени уменьшается после внутрисуставной инъекции с местным анестетиком, даже если это происходит в течение нескольких часов, можно сделать вывод, что существенная часть боли у пациента вызвана внутрисуставным источником.
Использовании местных анестетиков в смеси с кортикостероидами не лишено ряда недостатков. Многие лабораторные исследования показывают, что как кортикостероиды, так и местные анестетики могут быть хондротоксичными, как независимо друг от друга, так и при совместном использовании. [19, 20] Клинические данные, касающиеся хондролиза из-за внутрисуставного введения местного анестетика, в основном связаны с непрерывными инфузиями в плечевой сустав после операции на нем, но описаны и случаи с поражением коленного сустава.
В систематическом обзоре, посвященном влиянию местного анестетика на суставной хрящ, были обнаружены 167 клинических случаев, причем 163 (97,7%) случаев включали непрерывную инфузию местного анестетика для облегчения боли с помощью помпы, и бупивакаин, лидокаин, ропивакаин и левобупивакаин характеризовались некоторой токсичностью в отношении хряща. [20]
Нежелательные эффекты, связанные с местными анестетиками, смешанными в одной внутрисуставной инъекции со стероидов, могут не иметь клинического значения по сравнению с инфузионными помпами, но клинические данные ограничены, а рандомизированных контролируемых исследований нет, поэтому медицинские работники должны, по крайней мере, знать о хондротоксическом эффекте, наблюдавшемся в лабораторных исследованиях. Клинические данные, касающиеся хондротоксического потенциала, будут обсуждаться далее в этой статье.
Проблема, которая упоминалась в литературе при комбинировании стероидов с местными анестетиками, заключается в кристаллизации или образовании хлопьев. [4,9] Это явление связано с pH и размером частиц в растворе. [21] Клинические и in vivo эффекты такой кристаллизации неизвестны. Она может снижать биодоступность местного анестетика или влиять на эффективность кортикостероида. Некоторые медицинские работники вводят анестетик отдельно от кортикостероида, заменяя шприцы без извлечения иглы из сустава, чтобы снизить риск этого явления.
Место инъекции и вероятность введения препарата в сустав
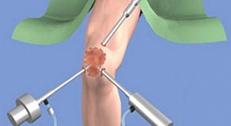
Разработано множество подходов для выполнения внутрисуставной инъекции в коленный сустав. [22] Обычные места для инъекций включают стандартный переднелатеральный и переднемедиальный артроскопический доступ (Рисунок 1). Кроме того, выделяют перипателлярные доступы, в том числе участок медиальнее или латеральнее середины надколенника и участок медиально или латерально сверху надколенника (Рисунок 2).
Рисунок 1. Фотография, на которой показаны AL и AM места инъекции, используемые в согнутом положении коленного сустава. AL = переднелатеральный, AM = переднемедиальный
Рисунок 2. Фотография, на которой показаны SL, SM, LMP и MMP места инъекции, используемые в разогнутом положении коленного сустава. LMP = латерально от середины надколенника, MMP = медиально от середины надколенника, SL = верхнелатеральный, SM = верхнемедиальный
Внешних ориентиров для инъекций нет, и были опубликованы различные показатели успешности фактической внутрисуставной инъекции по сравнению с внесуставной инъекцией в разных участках, составлявшие от 55% до 93%. [22,23]
Перипателлярные инъекции выполняются в разогнутом положении коленного сустава, и их недостатком является риск травмы хряща надколенника, особенно при инъекции на уровне середины надколенника, потому что игла должна пройти под надколенником, чтобы попасть в коленный сустав.
Выполнение инъекций выше надколенника имеет преимущество, так как там находится супрапателлярная суставная сумка, и игла не должна проходить под коленной чашечкой. Инъекции в передние участки выполняются в согнутом положении коленного сустава, поэтому пациент может сидеть.
Выбор места инъекции осуществляет медицинский работник, но пациентам можно предложить сидеть или лежать, и в зависимости от выбора пациента могут использоваться передние или перипателлярные участки инъекции.
Методы для повышения точности внутрисуставных инъекций в коленный сустав включают аспирацию жидкости перед инъекцией или использование визуализации, например, ультразвукового исследования или рентгеноскопии. Аспирация перед инъекцией является самым дешевым и быстрым методом подтверждения того, что игла находится внутри сустава; однако, если в коленном суставе нет значительного количества выпота, эта методика может быть неэффективной и ненадежной.
Недавно положении коленного сустава [24] описал метод, улучшающий успешность внутрисуставных инъекций в коленный сустав даже при отсутствии выпота и без необходимости визуализации. Его методика включает использование переднелатерального доступа при полностью согнутом коленном суставе и направление иглы латерально, а не к межмыщелковому углублению. При смещении бедренной кости назад, когда коленный сустав полностью согнут, а большеберцовая кость ротирована кнутри, объем латерального пространства увеличивается, что позволяет достичь точности 97,1% (P = 0,000). [24]
Среди всех методов визуализации, используемых при внутрисуставных инъекциях в коленный сустав, ультразвуковой контроль имеет преимущество за счет неионизирующего излучения, сравнительной дешевизны и простоты при применении в амбулаторных условиях.
Обзор исследований инъекций в коленный сустав под контролем УЗИ показал более высокую точность при использовании УЗИ по сравнению с тактильными инъекциями без визуализации (95,8% в сравнении 77,8% соответственно; P <0,001). [25] Повышенная внутрисуставная точность может привести к улучшению результатов лечения пациентов. Sibbitt et al [26] провели рандомизированное контролируемое исследование 94 коленных суставов без выпота, сравнив внутрисуставные инъекции кортикостероидом под ультразвуковым или анатомическим контролем, и обнаружили, что ультразвуковой контроль приводил к уменьшению боли при введении иглы на 48% (P = 0,0003), увеличению продолжительности терапевтического эффекта на 36% (P = 0,01) и к уменьшению боли в коленном суставе через 2 недели на 42% (P = 0,025), но через 6 месяцев различий уже не было (P = 1,0).
Точность в достижении внутрисуставной инъекции кортикостероида для лечения симптоматического остеоартрита представляется очевидно важной, но некоторые данные оспаривают эту идею. Hirsch et al [27] провели наблюдательное исследование, сравнивающее точность внутрисуставных инъекций стероидов с кратковременным облегчением боли. Они обнаружили, что приблизительно у 60% пациентов через 3 недели и у 45% пациентов через 9 недель отмечалось уменьшение количества баллов по шкале оценки боли Индекса выраженности остеоартрита университетов Западного Онтарио и МакМастера (Western Ontario and McMaster Universities Arthritis Index, WOMAC) на 40% и более по сравнению с исходным значением. Тем не менее, точно выполненная внутрисуставная инъекция кортикостероида по сравнению с внесуставной инъекцией не была взаимосвязана с уменьшением показателей выраженности боли (P = 0,389 через 3 недели и P = 0,365 через 9 недель). [27]
Обработка места инъекции и техника выполнения
Стерильность при выполнении внутрисуставных инъекций имеет важное значение; однако медицинские работники используют разные методы для достижения этой стерильности, и, по-видимому, единого мнения по поводу стандартных методов нет. [28,29]
Обычно используемые кожные антисептики включают изопропиловый спирт, хлоргексидин и повидон-йод. Некоторые медицинские работники используют стерильные перчатки, если касаются места инъекции после его обработки, тогда как другие применяют технику без прикосновения и надевают нестерильные перчатки. Charalambous et al [28] опросили медицинских работников в Великобритании относительно их практики внутрисуставных инъекций стероидов в коленный сустав и обнаружили, что 57,6% респондентов использовали только спиртовые салфетки, тогда как остальные применяли для обработки место инъекции либо бетадин, либо хлоргексидин.
Полные антисептические методы, включающие использование дезинфицирующих средств, стерильных перчаток и стерильного операционного белья для создания стерильного поля и использование второй иглы для извлечения лекарственного препарата, применяли только 13% респондентов, тогда как 53,4% опрошенных медицинских работников не надевали никаких перчаток, даже нестерильных. [28]
Несмотря на то, что стерильные перчатки не требуются благодаря использованию стерильной техники без прикосновения, универсальные меры предосторожности с применением средств индивидуальной защиты включают и рекомендуют медицинским работникам надевать нестерильные перчатки. Стерильные перчатки могут быть в 50 раз дороже, чем нестерильные, и их экономическая эффективность не установлена. [29]
Несмотря на отсутствие клинических данных относительно обработки кожи для внутрисуставной инъекции в коленный сустав, были опубликованы исследования, посвященные венепункции, которые можно использовать в качестве руководства.
В рандомизированном исследовании 2% спиртового раствора хлоргексидина по сравнению с 10% водным раствором повидон-йода для дезинфекции места венепункции с целью взятия крови для микробиологического исследования хлоргексидин оказался лучше: частота контаминации посевов крови составила 3,2% по сравнению с 6,9% при использовании повидон-йода (P <0,001). [30] Авторы отмечают, что максимальный антисептический эффект повидон-йода достигается через 1,5-2 минуты, тогда как хлоргексидину требуется всего 30 секунд для достижения максимального антисептического эффекта, поэтому короткое время высыхания антисептика могло повлиять на результаты. Кроме того, хлоргексидин не обязательно является лучшим антисептиком.
Недавно Martínez et al [31] провели слепое рандомизированное исследование, в котором сравнивали частоту контаминации посевов крови при использовании 70% изопропилового спирта и 2% хлоргексидина в качестве кожного антисептика и не обнаружили различий (0,9% по сравнению с 1,9% соответственно; P = 0,3). Поэтому лучшее дезинфицирующее средство для кожи пока не определено.
Еще один аспект включает распространенную практику использования хлорэтила в качестве местного анестезирующего спрея. Хлорэтила является хладагентом, поэтому он охлаждает кожу и уменьшает боль от прокола иглы. Существуют некоторые риски его использования, потому что это нестерильный спрей, и некоторые медицинские работники будут повторно обрабатывать кожу дезинфицирующим средством после нанесения хлорэтила. Polishchuk et al [32] провели проспективное слепое контролируемое исследование, сравнивающее рост микроорганизмов из образцов кожи до обработки спиртом, после обработки спиртом, но до применения хлорэтила и после применения хлорэтила.
Статистически значимых различий между ростом бактерий в образцах, взятых после обработки кожи спиртом, но до применения хлорэтила и после применения хлорэтила обнаружено не было (3% в сравнении с 5% соответственно; P = 0,65). Спрей с хлорэтилом наносили непосредственно на пустые чашки Петри и бульонную культуру и сравнивали с контролем (без применения спрея). Статистически значимых различий в росте бактерий обнаружено не было (P = 0,80). [32]
При наличии суставного выпота медицинские работники могут рассмотреть целесообразность аспирации жидкости из коленного сустава перед инъекцией, чтобы обеспечить дополнительное облегчение боли и улучшить подвижность сустава. Leung et al [33] провели ретроспективное предварительное исследование и обнаружили пользу от аспирации жидкости из коленного сустава перед инъекцией стероида при остеоартрите; однако улучшение, о котором сообщали пациенты, было более выражено в группе, где выполняли только инъекции.
Gaffney et al [34], наоборот, в своем рандомизированном проспективном плацебо-контролируемом исследовании обнаружили статистически значимое преимущество, о котором сообщали пациенты через 1 неделю, при выполнении аспирации с последующей инъекцией стероида по сравнению с отсутствием аспирации (92% по сравнению с 61%; P <0,05). Это преимущество сохранялось через 6 недель, при этом о нем сообщали 66% пациентов, которым выполняли аспирацию, и 44% пациентов, которым не выполняли аспирацию (статистическая значимость не указана).
Если перед инъекцией стероида выполняется аспирация, показания для анализа жидкости включают подозрение на воспалительный артрит или кристаллическую артропатию. Анализ жидкости также необходим при подозрении на септический артрит, и в этой ситуации стероид вводить не следует.
Последующие инъекции
Данных для создания практических рекомендаций относительно частоты и общего количества инъекций недостаточно. Общая рекомендация заключается в том, что в течение года следует выполнять не более 3–4 инъекций стероидов в коленный сустав, хотя, по-видимому, это основано на мнении специалистов, и есть различные точки зрения. [5,9,11] Безопасное максимальное количество инъекций стероидов в коленный сустав в течение жизни также неизвестно. Длительное повторное внутрисуставное введение стероидов для лечения симптоматического остеоартрита коленного сустава в целом оказалось неэффективным [35]. Пациентам можно объяснить, что количество инъекций стероидов в коленный сустав в течение жизни зависит от того, как долго лечение обеспечивает облегчение боли без побочных эффектов.
Liu et al [36] провели продольное исследование использования внутрисуставных инъекций у пациентов с остеоартритом коленного сустава. Они обнаружили, что в течение 9 лет приблизительно 59% пациентов, которым была выполнена первоначальная инъекция кортикостероида в коленный сустав, не получали дополнительных инъекций, и приблизительно 18% пациентов были переведены на инъекции гиалуроновой кислоты. Следовательно, последующие инъекции стероидов были выполнены только у немногим более 20% пациентов после первого введения кортикостероидов. Авторы обсуждают, как перевод на другой вид лечения в сравнении с продолжением или прекращением лечения у пациентов с хроническим заболеванием может быть связан с недостаточной эффективностью, проблемами безопасности или переносимостью лечения [36].
Результаты лечения
Было показано, что инъекции кортикостероидов в коленный сустав для лечения остеоартрита статистически и клинически значимо уменьшают боль в краткосрочной перспективе. [14,37-39] Однако точная длительность обезболивания остается неясной. Hepper et al [14] провели систематический обзор опубликованных в 2009 году исследований I уровня и обнаружили, что инъекции кортикостероидов для лечения боли, связанной с остеоартритом коленного сустава, приводили к статистически и клинически значимому облегчение боли через 1 неделю после инъекции.
По-видимому, в краткосрочной перспективе после 1 недели тоже было какое-то преимущество, но данные не были статистически значимыми по сравнению с плацебо. Обновление Кохрейновского обзора в 2015 году подтвердило этот результат с выводом о том, что клинические эффекты внутрисуставных инъекций кортикостероидов в коленный сустав оставались неясными через 1–6 недель после инъекции из-за плохого качества данных [37].
Доказательств клинического эффекта через 6 месяцев после инъекции обнаружено не было. Исследования эго вопроса неоднородны, а высококачественных, сильных, плацебо-контролируемых проспективных рандомизированных исследований нет; Кохрейновский обзор 2015 года оценил качество данных как «низкое», что было определено как отсутствие достоверности результатов из-за их несогласованности на основании небольших исследований. [37]
Показатели отдельных пациентов и степень тяжести артрита могут влиять на эффективность инъекций. Недавно Matzkin et al [38] изучили когорту из 100 пациентов, которым вводили стероиды для лечения симптоматического остеоартрита коленного сустава, и обнаружили улучшение показателей WOMAC (P <0,001) и оценки по визуальной числовой шкале (P <0,05) через 3, 6, 12 и 24 недели после инъекции, за исключением оценки по визуальной числовой шкале через 24 недели (P = 0,114), по сравнению с исходными значениями.
Однако у пациентов с ожирением в начале исследования показатели WOMAC были статистически значимо хуже по сравнению с пациентами без ожирения (P = 0,003) через 6 недель после инъекции (P = 0,010) и через 3 месяца после инъекции (P = 0,009), хотя и отмечалось улучшение по сравнению с исходным уровнем. У пациентов с более тяжелым артритом (3 или 4 степень по классификации Келлгрена-Лоуренса (Kellgren-Lawrence)) показатели были статистически значимо хуже через 6 недель после инъекции (P = 0,028) и через 3 месяца после инъекции (P = 0,004), хотя также отмечалось улучшение по сравнению с исходным уровнем.
Maricar et al [39] наблюдали за группой из 207 пациентов и описали структурные предикторы клинического ответа на внутрисуставные инъекции стероидов при симптоматическом остеоартрите коленного сустава. Они обнаружили, что 73,4% пациентов ответили на лечение быстро - через 2 недели и 20,1% ответили на лечение в долгосрочной перспективе - через 6 месяцев после инъекции.
Структурные предикторы быстрого ответа найдены не были, но они были обнаружены при долгосрочном ответе. Рентгенографическое ухудшение заболевания, включая усиление общего сужения суставного пространства (P = 0,047) и общая оценка по классификации Келлгрена-Лоуренса (P = 0,010), были взаимосвязаны с отсутствием долгосрочного ответа [39].
Maricar et al [40] также провели систематический обзор предикторов ответа на инъекции стероидов в коленные суставы при остеоартрите и обнаружили повышенную вероятность ответа у пациентов с выпотом, отсутствием синовита, более выраженными исходными симптомами и менее тяжелым заболеванием на рентгенограммах, а также у пациентов, которым выполняли инъекцию под контролем УЗИ.
Как отмечалось ранее, одной из проблем, связанных с повторными инъекциями, является хондротоксичность. В литературе опубликованы смешанные результаты исследований возможного влияния внутрисуставных инъекций стероидов на естественное течение остеоартрита коленного сустава, ускоряя разрушение хряща. В 2017 году McAlindon et al [35] опубликовали рандомизированное плацебо-контролируемое двойное слепое исследование 140 пациентов, которым выполняли либо инъекцию стероидов, либо инъекцию физиологического раствора каждые 3 месяца в течение 2 лет, и показали увеличение потери объема хряща коленного сустава, согласно оценке с помощью МРТ, и неоднозначную оценку боли за два года наблюдения у пациентов, получавших инъекции стероидов, по сравнению с теми, кто получал плацебо. В этом исследовании клинические последствия потери хряща, измеренной с помощью МРТ, неизвестны, особенно у пациентов с уже имеющимся обширным повреждением хрящевой ткани. Расчетная потеря хряща, соответствующая используемому индексу МРТ, составила 0,46 мм, а значение для минимально клинически значимого различия еще не установлено [35].
Исследованию McAlindon et al можно противопоставить рандомизированное двойное слепое плацебо-контролируемое исследование Raynauld et al [41], в котором в коленные суставы вводили стероиды для лечения остеоартрита каждые 3 месяца в течение 2 лет и измеряли сужение суставного пространства на рентгенограммах наряду с результатами, сообщаемыми пациентами. В течение одного и двух лет наблюдения не было обнаружено статистически значимых различий в рентгенологическом сужении суставного пространства с течением времени. В течение двух лет наблюдения не было обнаружено статистически значимых различий в уменьшении боли, но при использовании анализа области под кривой для описания изменений в результатах лечения на протяжении всего исследования у пациентов, получавших инъекции стероидов. боль статистически значимо улучшалась (P = 0,0047), как и показатели ригидности (P = 0,0511). [41]
Внутрисуставные инъекции редко бывают эффективными в качестве долгосрочной стратегии лечения симптоматического остеоартрита коленного сустава. Последующие инъекции часто хуже облегчают боль, или их эффект оказывается менее продолжительным. Hirsch et al [27] обнаружили, что у пациентов, которые ранее получали внутрисуставные инъекции стероидов, вероятность достижения эффекта была меньше через 9 недель (P = 0,021), но не через 3 недели (P = 0,314) после инъекции, чем у пациентов, которым впервые выполняли инъекцию. Исследование, проведенное Raynauld et al, показало аналогичные результаты, так как результаты оценки боли через два года статистически значимо не различались у пациентов, получавших плацебо по сравнению со стероидами; однако при анализе площади под кривой, общие показатели выраженности боли в течение 2 лет были статистически значимо ниже у пациентов, получивших инъекцию стероида (P = 0,0047).
Психосоматические влияния и эффект плацебо также могут играть важную роль в лечении хронических болевых состояний. [5] В мета-анализе пероральных и внутрисуставных препаратов для лечения остеоартрита коленного сустава проанализировали 137 исследований, включавших 33243 пациента, и было обнаружено, что внутрисуставное введение плацебо статистически значимо лучше уменьшало боль, чем пероральное плацебо (величина эффекта 0,29 [доверительный интервал 95%, 0,04-0,54]), и ни один из пероральных нестероидных противовоспалительных препаратов статистически значимо не превосходил внутрисуставное плацебо. [42]
Нежелательные эффекты и осложнения
Внутрисуставные инъекции кортикостероидов в коленный сустав считаются относительно безопасной процедурой. В Кохрейновском обзоре показано, что инъекции коленный сустав в колено вызывают столько же нежелательных эффектов, как и плацебо (13% и 15% соответственно). [37] Противопоказания (Таблица 2) включают аллергию на вводимый препарат и наличие активной инфекции сустава. Внутрисуставную инъекцию коленного сустава следует с большей осторожностью выполнять при коагулопатиях или инфекциях коленного сустава, а также при артропластике коленного сустава. Местные нежелательные эффекты (Таблица 3) включают изменения пигментации кожи в месте инъекции, атрофию жировой ткани или кожи и остаточную боль в месте инъекции. [4] Также возможно прямое повреждение хряща иглой, особенно при использовании для инъекции латерального или медиального доступа н уровне середины надколенника.
Таблица 2. Относительные противопоказания к внутрисуставным инъекциям кортикостероидов
|
|
Относительные противопоказания
|
|
Аллергия на кортикостероид
|
|
Активная местная или системная инфекция
|
|
Коагулопатия
|
|
Поражение кожи
|
|
Перелом
|
|
Наличие протеза сустава
|
|
Лабильный сахарный диабет
|
Таблица 3. Возможные нежелательные эффекты и осложнения внутрисуставных инъекций кортикостероидов
|
|
Нежелательные эффекты и осложнения
|
|
Изменения пигментации кожи
|
|
Атрофия жировой ткани или кожи
|
|
Остаточная боль в месте инъекции
|
|
Покраснение лица
|
|
Подавление функции гипоталамо-гипофизарно-надпочечниковой оси
|
|
Повышение уровня глюкозы в крови
|
|
Септический артрит
|
|
Прямое повреждение хряща иглой
|
Внутрисуставные инъекции кортикостероидов могут вызывать такие же системные эффекты (Таблица 3), как и пероральные или внутривенные стероиды, но при внутрисуставном введении системные проявления, как правило, менее тяжелые.
Возможные системные эффекты включают покраснение лица, подавление функции гипоталамо-гипофизарно-надпочечниковой оси и усиление синтеза глюкозы в печени, что приводит к повышению уровня глюкозы в крови. [4] Повышение уровня глюкозы, как правило, имеет самое большое значение для пациентов с сахарным диабетом, и они должны знать, что после инъекции стероидов концентрация глюкозы в крови может увеличиваться.
Другие возможные побочные эффекты включают стероидную миопатию и остеонекроз. Насколько нам известно, в литературе не опубликовано сообщений об этих эффектах в связи с внутрисуставной инъекцией стероида в коленный сустав.
Наиболее опасным осложнением, связанным с инъекциями кортикостероидов в коленный сустав, является септический артрит. Его частота составляет от 1 на 3000 до 1 на 50000 [4]. Xu et al [43] провели ретроспективное исследование случай-контроль, изучив 50 глубоких инфекций коленного сустава после внутрисуставных инъекций по сравнению с 250 лицами из группы контроля.
Было установлено, что статистически значимыми факторами риска развития септического артрита коленного сустава, связанного с внутрисуставной инъекцией, являются индекс массы тела пациента более 25 кг/м2 (отношение шансов 2,3; 95% доверительный интервал от 1,1 до 4,7), выполнение инъекции врачом общей практики по сравнению с хирургом-ортопедом или ревматологом (отношение шансов 5,23; 95% доверительный интервал от 2,00 до 13,67) и наличие ревматоидного артрита (отношение шансов 2,61; 95% доверительный интервал от 1,20 до 5,68). Инъекции кортикостероидов были статистически значимым фактором риска по сравнению с инъекциями гиалуроновой кислоты (отношение шансов 3,21; 95% доверительный интервал от 1,63 до 6,31). [43]
Многим пациентам, которые получают инъекции кортикостероидов для лечения остеоартрита коленного сустава, в конечном итоге часто приходится выполнять тотальную артропластику коленного сустава (ТАКС). Недавних был опубликован ряд исследований, посвященных риску инфекции, связанной с инъекциями стероидов до ТАКС. В 2016 году Amin et al [44] ретроспективно изучили 1628 пациентов в течение семилетнего периода, которые либо получали, либо не получали внутрисуставную инъекцию перед выполнением ТАКС, и не обнаружили никакой корреляции с пациентами, у которых развились инфекционные осложнения тотальной артропластики коленного сустава и была выполнена инъекция кортикостероида перед операцией (относительный риск инъекции стероида по сравнению с контрольной группой 0,9389; P = 0,9146).
Тем не менее, сроки проведения инъекций могут повлиять на риск перипротезной инфекции сустава при ТАКС. Cancienne et al [45] выполнили большое исследование базы данных и не обнаружили статистически значимых различий в инфекциях при ТАКС у пациентов, которые получили инъекцию в коленный сустав более чем за 3 месяца до операции. Тем не менее, у пациентов, которым была выполнена ТАКС в течение 3 месяцев после инъекции в коленный сустав, частота инфицирования была статистически значимо повышена через 3 месяца (2,6%; отношение шансов 2,0; доверительный интервал от 1,6 до 2,5; P <0,0001) и через 6 месяцев (3,41% отношение шансов 1,5; доверительный интервал от 1,2 до 1,8; P <0,0001) после ТАКС. [45] Таким образом, может быть полезно выполнять ТАКС не менее чем через 3 месяца после инъекции в коленный сустав.
Заключение
Внутрисуставные инъекции стероидов являются относительно безопасным методом лечения для кратковременного уменьшения симптомов остеоартрита коленного сустава. Их не следует выполнять регулярно, а использовать только в тех случаях, когда у пациентов есть существенные симптомы. Внутрисуставные инъекции стероидов следует прекратить, если предыдущие инъекции не обеспечили существенного облегчения. Недавние исследования показывают, что при многочисленных последующих инъекциях возможна потеря хряща, хотя клинические эффекты неизвестны и могут не иметь значения у пациентов с выраженным остеоартритом. Медицинские работники и пациенты должны знать о рисках и возможных осложнениях этого частого метода лечения.