Арбидол и COVID-19
Список клинических исследований арбидола в отношении коронавирусной инфекции.
Прежде чем перейти к рассмотрению клинических исследований (КИ), необходимо понять на каких основаниях арбидол стал рассматриваться в качестве перспективной молекулы против коронавирусов. То есть обратимся к доклинике.
По моим представлениям доклиника - это исследования:
- in silico,
- in vitro,
- исследования на животных.
- In silico:
1.1. Analysis of therapeutic targets for SARS-CoV-2 and discovery of potential drugs by computational methods
Авторы: Canrong Wu, Yang Liu, Yueying Yang, Peng Zhang, Wu Zhong, Yali Wang, Qiqi Wang, Yang Xu, Mingxue Li, Xingzhou Li, Mengzhu Zheng, Lixia Chen, Hua Li.
Степень конгруэнтности при молекулярном докинге вещества оценивается по величине mfScores. Если эта величина меньше -100, то исследуемое вещество обладает сильным взаимодействием с конкретной молекулой. Ниже приведены молекулы коронавируса, с которыми может взаимодействовать арбидол (в скобках приведено аналогичное значение для фавипиравира):
−136.087 - комплекс неструктурных белков Nsp7_Nsp8
−118.253 - Nsp14
−118.253 - Nsp15
−117.879 (−107.889) - ионный канал E-белков
−145.125 - S-белок
1.2. Arbidol: A potential antiviral drug for the treatment of SARS-CoV-2 by blocking the trimerization of viral spike glycoprotein?
Автор: Naveen Vankadari
Арбидол может блокировать тримеризацию S-белка вируса.
In vitro:
2.1. The Experimental Study of the Anti-SARS-CoV Effect of Arbidole
Арбидол может блокировать тримеризацию S-белка вируса.
In vitro:
2.1. The Experimental Study of the Anti-SARS-CoV Effect of Arbidole
Авторы: Xiao-Guang Ji, Yan-Hong Zhao, Min Zhang, Jing-Hua Zhao, Jing-Yan Wang.
На перевиваемой линии клеток почек зеленых мартышек Vero-E6 сравнивали эффекты арбидола и рибавирина.
Концентрация полумаксимального ингибирования, IC50 (концентрации исследуемого вещества, необходимого для 50 % ингибирования тестовой реакции in vitro): 7.41 мкг/мл (арбидол), 66.1 мкг/мл (рибавирин).
Терапевтический индекс, ТИ (летальная доза препарата для 50 % клеток разделенная на минимальную эффективную дозу для 50 % клеток): 1.77 (арбидол), 6.1 (рибавирин).
2.2. The anti-influenza virus drug, arbidol is an efficient inhibitor of SARS-CoV-2 in vitro
Авторы: Xi Wang, Ruiyuan Cao, Huanyu Zhang, Jia Liu, Mingyue Xu, Hengrui Hu, Yufeng Li, Lei Zhao, Wei Li, Xiulian Sun, Xinglou Yang, Zhengli Shi, Fei Deng, Zhihong Hu, Wu Zhong & Manli Wang
Арбидол эффективно ингибировал вирус in vitro. Полумаксимальная эффективная концентрация, EC50 и 50% цитотоксическая концентрация (CC50) арбидола составляли 4.11 (3.55–4.73) и 31.79 (29.89–33.81) мкмоль соответственно, а индекс селективности (SI = CC50 / EC50) составил 7.73.
Модельные животные:
3.1. Analysis of Arbidol Efficiency against an Experimental form of Severe Acute Respiratory Syndrome
Авторы: С. Я. Логинова, В. Н. Щукина, С. В. Борисевич, Р. А. Хамитов, В. А. Максимов, А. М. Шустер.
“Результаты оценки противовирусной эффективности арбидола в отношении экспериментальной формы ТОРС у сирийских хомяков показывают, что при профилактическом применении препарата не выявлено значимого подавления репродукции вируса ТОРС в легких инфицированных животных... Лечебно-профилактическое пероральное применение арбидола на пике инфекции (4-е сутки) снижает уровень накопления вируса на 96–98%, к 10-м суткам наблюдения репродукция вируса практически полностью подавлялась препаратом.”
На перевиваемой линии клеток почек зеленых мартышек Vero-E6 сравнивали эффекты арбидола и рибавирина.
Концентрация полумаксимального ингибирования, IC50 (концентрации исследуемого вещества, необходимого для 50 % ингибирования тестовой реакции in vitro): 7.41 мкг/мл (арбидол), 66.1 мкг/мл (рибавирин).
Терапевтический индекс, ТИ (летальная доза препарата для 50 % клеток разделенная на минимальную эффективную дозу для 50 % клеток): 1.77 (арбидол), 6.1 (рибавирин).
2.2. The anti-influenza virus drug, arbidol is an efficient inhibitor of SARS-CoV-2 in vitro
Авторы: Xi Wang, Ruiyuan Cao, Huanyu Zhang, Jia Liu, Mingyue Xu, Hengrui Hu, Yufeng Li, Lei Zhao, Wei Li, Xiulian Sun, Xinglou Yang, Zhengli Shi, Fei Deng, Zhihong Hu, Wu Zhong & Manli Wang
Арбидол эффективно ингибировал вирус in vitro. Полумаксимальная эффективная концентрация, EC50 и 50% цитотоксическая концентрация (CC50) арбидола составляли 4.11 (3.55–4.73) и 31.79 (29.89–33.81) мкмоль соответственно, а индекс селективности (SI = CC50 / EC50) составил 7.73.
Модельные животные:
3.1. Analysis of Arbidol Efficiency against an Experimental form of Severe Acute Respiratory Syndrome
Авторы: С. Я. Логинова, В. Н. Щукина, С. В. Борисевич, Р. А. Хамитов, В. А. Максимов, А. М. Шустер.
“Результаты оценки противовирусной эффективности арбидола в отношении экспериментальной формы ТОРС у сирийских хомяков показывают, что при профилактическом применении препарата не выявлено значимого подавления репродукции вируса ТОРС в легких инфицированных животных... Лечебно-профилактическое пероральное применение арбидола на пике инфекции (4-е сутки) снижает уровень накопления вируса на 96–98%, к 10-м суткам наблюдения репродукция вируса практически полностью подавлялась препаратом.”
Клинические исследования арбидола
Согласно этой корреспонденции, на 24 апреля 2020 арбидол участвовал в 10 клинических исследованиях:
в 5 КИ препарат сравнивается со стандартной терапией (чтобы это не значило),
в 1 исследование - с калетрой,
в 1 - с фавипиравиром,
в 2 исследованиях - с интерфероном и интерфероном+арбидолом,
в 1 - с хлорохином.
A.1. Clinical Features of 69 Cases with Coronavirus Disease 2019 in Wuhan, China
Авторы: Zhongliang Wang, Bohan Yang, Qianwen Li, Lu Wen, and Ruiguang Zhang.
Это ретроспективное клиническое исследование.
Минусы: отсутствие рандомизации
Объем выборки: 69 пациентов.
12 (33%) из 36 пациентов были выписаны в группе, получавшей арбидол, тогда как только 6 (19%) из 31 пациента были выписаны в группе, не получавшей арбидол. Все смерти произошли в группе, не получавшей арбидол (0% [0/36] против 16% [5/31]).
A.2. ПРЕПРИНТ (публикация не проходила рецензирование). Potential of Arbidol for Post-exposure Prophylaxis of COVID-19 Transmission
Авторы: Jinnong Zhang, Wenjing Wang, Bo Peng, Wei Peng, Yisheng,Zhang, Yaling Wang, Yan Wan, Jiang Chang, Ling Mao, Xiaoping Miao, Yifan Zhou, Yanan Li, Yu Hu, Bo Hu.
Это ретроспективное клиническое исследование по типу случай-контроль (retrospective case-control study) для оценки потенциала арбидола в качестве постконтактной профилактики COVID-19.
Минусы: отсутствие рандомизации.
Объем выборки: 190 человек (66 членов семей и 124 медицинских работника).
Арбидол продемонстрировал защитный эффект против развития COVID-19 (отношение шансов 0.011, 95% ДИ 0.001-0.125, p = 0.0003 у членов семей и отношение шансов 0,049, 95% ДИ 0.003-0.717, p = 0.0276 у медицинских работников).
A.3. ПРЕПРИНТ. Clinical features and progression of acute respiratory distress syndrome in 2 coronavirus disease 2019
Авторы: Yanli Liu, Wenwu Sun, Jia Li, Liangkai Chen, Yujun Wang, Lijuan Zhang, Li Yu.
Это ретроспективное клиническое исследование выживаемости пациентов с ОРДС при COVID-19.
Минусы: отсутствие рандомизации.
Объем выборки: 53 пациента (арбидол получали 6 пациентов).
Результат (статистически не значимый, p = 0.19) на рисунке:
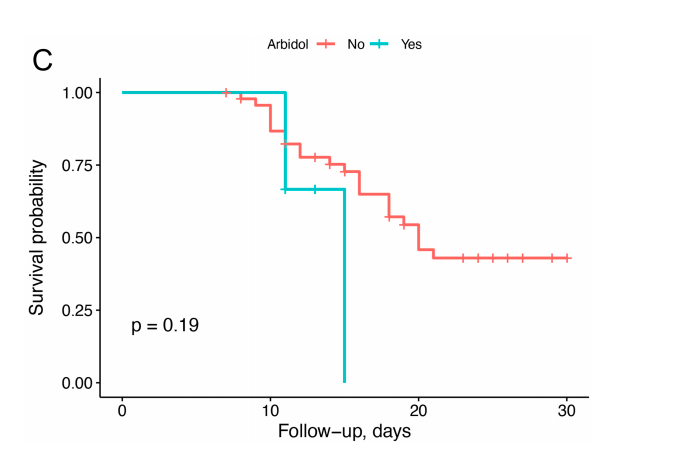
A.4. Umifenovir treatment is not associated with improved outcomes in patients with coronavirus disease 2019: A retrospective study
Авторы: N. Lian, H. Xie, S. Lin, J. Huang, J. Zhao, Q. Lin.
Это ретроспективное, контролируемое клиническое исследование эффективности арбидола у пациентов с COVID-19 вне ОРИТ.
Минусы: отсутствие рандомизации.
Объем выборки: 81 пациент (45 - арбидол, 36 - контроль).
Среднее время от момента госпитализации до первого отрицательного теста на SARS-CoV-2 было больше в группе арбидола, чем в контрольной группе (6 дней против 3 дней, p <0.05) Однако, среднее время от начала заболевания до даты первого отрицательного теста было сопоставимо в обеих группах (18 дней и 16 дней , p >0.05). Продолжительность пребывания в больнице была больше в группе арбидола, чем в контрольной группе (13 дней против 11 дней, р = 0.04) Пациенты с тяжелым течением заболевания, получавшие арбидол, чувствовали себя не лучше, чем пациенты с тяжелым течением в контрольной группе.
B.1. An exploratory randomized, controlled study on the efficacy and safety of lopinavir/ritonavir or arbidol treating adult patients hospitalized with mild/moderate COVID-19 (ELACOI)
Авторы: Yueping Li, Zhiwei Xie, Weiyin Lin, Weiping Cai, Chunyan Wen, Yujuan Guan, Xiaoneng Mo, Jian Wang, Yaping Wang, Ping Peng, Xudan Chen, Wenxin Hong, Guangming Xiao, Jinxin Liu, Lieguang Zhang, Fengyu Hu, Feng Li, Fuchun Zhang, Xilong Deng, Linghua Li.
Это рандомизированное (2:2:1), контролируемое клиническое исследование (randomized (2:2:1) controlled trial) оценивающее эффективность и безопасность монотерапии лопинавир/ритонавир (LPV/r) или арбидола для лечения пациентов с мягкой/умеренной формами COVID-19.
Протокол исследования NCT04252885 был предварительно зарегистрирован на clinicaltials, что соответствует требованиям CONSORT для рандомизированных исследований.
в 5 КИ препарат сравнивается со стандартной терапией (чтобы это не значило),
в 1 исследование - с калетрой,
в 1 - с фавипиравиром,
в 2 исследованиях - с интерфероном и интерфероном+арбидолом,
в 1 - с хлорохином.
A.1. Clinical Features of 69 Cases with Coronavirus Disease 2019 in Wuhan, China
Авторы: Zhongliang Wang, Bohan Yang, Qianwen Li, Lu Wen, and Ruiguang Zhang.
Это ретроспективное клиническое исследование.
Минусы: отсутствие рандомизации
Объем выборки: 69 пациентов.
12 (33%) из 36 пациентов были выписаны в группе, получавшей арбидол, тогда как только 6 (19%) из 31 пациента были выписаны в группе, не получавшей арбидол. Все смерти произошли в группе, не получавшей арбидол (0% [0/36] против 16% [5/31]).
A.2. ПРЕПРИНТ (публикация не проходила рецензирование). Potential of Arbidol for Post-exposure Prophylaxis of COVID-19 Transmission
Авторы: Jinnong Zhang, Wenjing Wang, Bo Peng, Wei Peng, Yisheng,Zhang, Yaling Wang, Yan Wan, Jiang Chang, Ling Mao, Xiaoping Miao, Yifan Zhou, Yanan Li, Yu Hu, Bo Hu.
Это ретроспективное клиническое исследование по типу случай-контроль (retrospective case-control study) для оценки потенциала арбидола в качестве постконтактной профилактики COVID-19.
Минусы: отсутствие рандомизации.
Объем выборки: 190 человек (66 членов семей и 124 медицинских работника).
Арбидол продемонстрировал защитный эффект против развития COVID-19 (отношение шансов 0.011, 95% ДИ 0.001-0.125, p = 0.0003 у членов семей и отношение шансов 0,049, 95% ДИ 0.003-0.717, p = 0.0276 у медицинских работников).
A.3. ПРЕПРИНТ. Clinical features and progression of acute respiratory distress syndrome in 2 coronavirus disease 2019
Авторы: Yanli Liu, Wenwu Sun, Jia Li, Liangkai Chen, Yujun Wang, Lijuan Zhang, Li Yu.
Это ретроспективное клиническое исследование выживаемости пациентов с ОРДС при COVID-19.
Минусы: отсутствие рандомизации.
Объем выборки: 53 пациента (арбидол получали 6 пациентов).
Результат (статистически не значимый, p = 0.19) на рисунке:

A.4. Umifenovir treatment is not associated with improved outcomes in patients with coronavirus disease 2019: A retrospective study
Авторы: N. Lian, H. Xie, S. Lin, J. Huang, J. Zhao, Q. Lin.
Это ретроспективное, контролируемое клиническое исследование эффективности арбидола у пациентов с COVID-19 вне ОРИТ.
Минусы: отсутствие рандомизации.
Объем выборки: 81 пациент (45 - арбидол, 36 - контроль).
Среднее время от момента госпитализации до первого отрицательного теста на SARS-CoV-2 было больше в группе арбидола, чем в контрольной группе (6 дней против 3 дней, p <0.05) Однако, среднее время от начала заболевания до даты первого отрицательного теста было сопоставимо в обеих группах (18 дней и 16 дней , p >0.05). Продолжительность пребывания в больнице была больше в группе арбидола, чем в контрольной группе (13 дней против 11 дней, р = 0.04) Пациенты с тяжелым течением заболевания, получавшие арбидол, чувствовали себя не лучше, чем пациенты с тяжелым течением в контрольной группе.
B.1. An exploratory randomized, controlled study on the efficacy and safety of lopinavir/ritonavir or arbidol treating adult patients hospitalized with mild/moderate COVID-19 (ELACOI)
Авторы: Yueping Li, Zhiwei Xie, Weiyin Lin, Weiping Cai, Chunyan Wen, Yujuan Guan, Xiaoneng Mo, Jian Wang, Yaping Wang, Ping Peng, Xudan Chen, Wenxin Hong, Guangming Xiao, Jinxin Liu, Lieguang Zhang, Fengyu Hu, Feng Li, Fuchun Zhang, Xilong Deng, Linghua Li.
Это рандомизированное (2:2:1), контролируемое клиническое исследование (randomized (2:2:1) controlled trial) оценивающее эффективность и безопасность монотерапии лопинавир/ритонавир (LPV/r) или арбидола для лечения пациентов с мягкой/умеренной формами COVID-19.
Протокол исследования NCT04252885 был предварительно зарегистрирован на clinicaltials, что соответствует требованиям CONSORT для рандомизированных исследований.
Объем выборки: 125 пациента (34 - лопинавир/ритонавир (калетра), 35 - арбидол, 17 - контроль).
Результаты:
B.2. Efficacies of lopinavir/ritonavir and arbidol in the treatment of novel coronavirus pneumonia
Авторы: Chen Jun, Ling Yun, Xi Xiuhong, Liu Ping, Li Feng, Li Tao, Shang Zhiyin, Wang Mei, Shen Yinzhong, Lu Hongzhou
Это ретроспективное, контролируемое, сравнительное клиническое исследование эффективности лопинавира/ритонавира и арбидола в лечении новой коронавирусной пневмонии.
Минусы: отсутствие рандомизации.
Объем выборки: 134 пациента (52 - лопинавир/ритонавир (калетра), 34 - арбидол, 48 - контроль).
Выводы: Это исследование не обнаружило какого-либо влияния лопинавира / ритонавира и арбидола на уменьшение симптомов или ускорения снижения вирусной нагрузки.
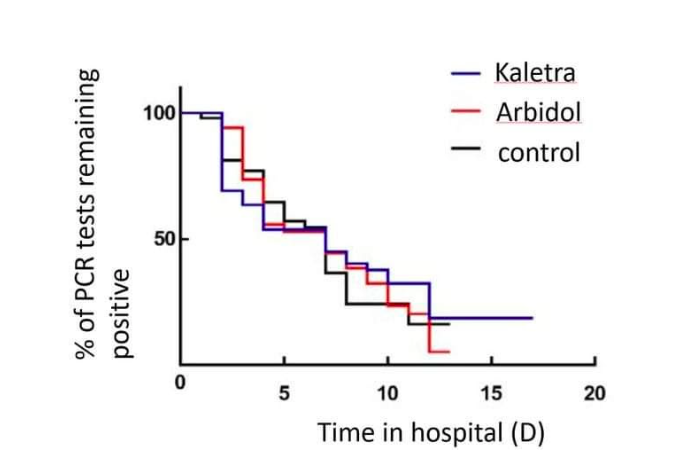
B.3. Arbidol monotherapy is superior to lopinavir/ritonavir in treating COVID-19
Авторы: Zhen Zhu, Zhaohui Lu, Tianmin Xu, Cong Chen, Gang Yang, Tao Zha, Jianchun Lu, Yuan Xue.
Это ретроспективное сравнительное клиническое исследование эффективности и безопасности монотерапии лопинавир/ритонавир и арбидола у пациентов с COVID-19.
Минусы: отсутствие рандомизации.
Объем выборки: 50 пациентов (34 - лопинавир/ритонавир, 16 - арбидол).
Результаты:
C.1. ПРЕПРИНТ. Favipiravir versus Arbidol for COVID-19: A Randomized Clinical Trial
Авторы: Chang Chen, Yi Zhang, Jianying Huang, Ping Yin, Zhenshun Cheng, Jianyuan Wu, Song Chen, Yongxi Zhang, Bo Chen, Mengxin Lu, Yongwen Luo, Lingao Ju, Jingyi Zhang, Xinghuan Wang
Это проспективное, рандомизированное, контролируемое, открытое, многоцентровое клиническое исследование (prospective, randomized, controlled, open-label multicenter trial).
Предварительную регистрацию протокола я не нашел (только на китайском аналоге ГРЛС).
Объем выборки: 240 пациентов (120 - фавипиравир, 120 - арбидол).
Результаты:
- Эффективность: не было существенных различий в результатах лечения среди этих трех групп в этом исследовании. Не было обнаружено статистических различий между тремя группами в показателях антипиреза, облегчения кашля, улучшениях на КТ грудной клетки или степени ухудшения клинического статуса (для всех p > 0.05).
- Безопасность: LPV/r может вызывать больше нежелательных явлений. 5 (23.8%) пациентов в группе LPV/r испытали нежелательные явления в течение периода наблюдения. В группе арбидола или контрольной группе явных нежелательных явлений не наблюдалось.
B.2. Efficacies of lopinavir/ritonavir and arbidol in the treatment of novel coronavirus pneumonia
Авторы: Chen Jun, Ling Yun, Xi Xiuhong, Liu Ping, Li Feng, Li Tao, Shang Zhiyin, Wang Mei, Shen Yinzhong, Lu Hongzhou
Это ретроспективное, контролируемое, сравнительное клиническое исследование эффективности лопинавира/ритонавира и арбидола в лечении новой коронавирусной пневмонии.
Минусы: отсутствие рандомизации.
Объем выборки: 134 пациента (52 - лопинавир/ритонавир (калетра), 34 - арбидол, 48 - контроль).
Выводы: Это исследование не обнаружило какого-либо влияния лопинавира / ритонавира и арбидола на уменьшение симптомов или ускорения снижения вирусной нагрузки.

B.3. Arbidol monotherapy is superior to lopinavir/ritonavir in treating COVID-19
Авторы: Zhen Zhu, Zhaohui Lu, Tianmin Xu, Cong Chen, Gang Yang, Tao Zha, Jianchun Lu, Yuan Xue.
Это ретроспективное сравнительное клиническое исследование эффективности и безопасности монотерапии лопинавир/ритонавир и арбидола у пациентов с COVID-19.
Минусы: отсутствие рандомизации.
Объем выборки: 50 пациентов (34 - лопинавир/ритонавир, 16 - арбидол).
Результаты:
- Эффективность: Пациенты в группе арбидола имели более короткую продолжительность положительного теста РНК по сравнению с группой лопинавир/ритонавир (p < 0.01).
- Безопасность: У одного пациента в группе лопинавира/ритонавира и двух пациентов в группе арбидола была диагностирована лейкопения при госпитализации.
C.1. ПРЕПРИНТ. Favipiravir versus Arbidol for COVID-19: A Randomized Clinical Trial
Авторы: Chang Chen, Yi Zhang, Jianying Huang, Ping Yin, Zhenshun Cheng, Jianyuan Wu, Song Chen, Yongxi Zhang, Bo Chen, Mengxin Lu, Yongwen Luo, Lingao Ju, Jingyi Zhang, Xinghuan Wang
Это проспективное, рандомизированное, контролируемое, открытое, многоцентровое клиническое исследование (prospective, randomized, controlled, open-label multicenter trial).
Предварительную регистрацию протокола я не нашел (только на китайском аналоге ГРЛС).
Объем выборки: 240 пациентов (120 - фавипиравир, 120 - арбидол).
Привожу результаты c p-уровнем значимости < 0.05 (не забываем про его неправильное употребление).
Заключение
Существует мнение, что пока арбидол не доказал обратное в РКИ, его нужно считать потенциально небезопасным. Но он уже сделал это в исследовании АРБИТР:
- Для обычных пациентов с COVID-19 частота выздоровления за 7 дней составила 55.86% (62/111) в группе арбидола и 71.43% (70/98) в группе фавипиравира (p = 0.0199).
- Для обычных пациентов с COVID-19 время снижения температуры и облегчения кашля в группе фавипиравира было значительно короче, чем в группе арбидола (p < 0.0001).
- Для пациентов с COVID-19 с артериальной гипертензией и / или диабетом время снижения температуры и облегчения кашля в группе фавипиравира также было значительно короче, чем в группе арбидола (p < 0.0001).
- Частота возникновения новой одышки в группе арбидола составила 11.67% (14/120), а в группе фавипиравира - 3.45% (4/116) при значении p = 0.0174.
- Наиболее частыми нежелательными явлениями были повышение уровня мочевой кислоты в сыворотке крови (3 [2.50%] против 16 [13.79%], р = 0.0014), чаще встречающееся у пациентов группы фавипиравира, чем у пациентов группы арбидола.
Заключение
Существует мнение, что пока арбидол не доказал обратное в РКИ, его нужно считать потенциально небезопасным. Но он уже сделал это в исследовании АРБИТР:
“Зарегистрировано 14 нежелательных явлений (AE) в группе умифеновира и 28 AE в группе плацебо.”
В заключение, чтобы поддержать традиционную фразу “Нужно больше РКИ!”, хочу упомянуть рандомизированное, открытое, многоцентровое клиническое исследование (randomized, open, multicenter clinical study) эффективности и безопасности арбидола у пациентов с пневмонией, у которых диагностирована инфекция 2019-ncov.
Протокол исследования NCT04260594 был предварительно зарегистрирован на clinicaltials, объем выборки - 380 пациентов.