Анафилаксия. Обзор для врачей
СОКРАЩЕНИЯ: альфа-гал = альфа-галактоза; ЭКЖ = экстракорпоральное жизнеобеспечение; ИА = идиопатическая анафилаксия; в/к = внутрикостно; НПВП = нестероидный противовоспалительный препарат; PAF = фактор активации тромбоцитов; ЛШМ = латеральная широкая мышца бедра
Анафилаксия и ангионевротический отек - серьезные нарушения, которые могут привести к смертельной обструкции дыхательных путей и завершиться остановкой сердца и дыхания, гипоксемией и/или шоком, требующими лечения в условиях отделения интенсивной терапии. [1-3]
Анафилаксия определяется как системная, немедленная реакция гиперчувствительности, опосредованная IgE и приводящая к высвобождению медиаторов из тучных клеток и базофилов. Это вызывает множественные клинические эффекты, которые и позволяют поставить диагноз (Таблица 1).
Модели анафилаксии: однофазная, двухфазная и отсроченная
Анафилаксия с летальным исходом и время до смерти
|
Анафилаксия высоко вероятна, если соблюдено хотя бы одно из следующих трех условий. | |
|
1. |
Острое начало со следующими признаками: |
|
|
Поражение кожи и слизистых оболочек (зуд, приливы крови к лицу, крапивница, ангионевротический отек) и один из следующих признаков: |
|
|
A. Респираторные осложнения (хрипы, стридор, гипоксемия / цианоз) |
|
|
B. Артериальная гипотензияа или повреждение органов-мишеней (энцефалопатия, повреждение почек и т. д.) |
|
2. |
Два или более из следующих признаков, которые быстро появляются после воздействия известного или вероятного аллергена: |
|
|
|
|
|
|
|
|
|
|
|
|
|
3. |
Снижение АД вскоре после воздействия известного аллергена. |
Эпидемиология: распространенность, госпитализация и анафилактический шок
Механизмы анафилаксии
Эти триггеры приводят к активации каскада передачи сигналов, кульминацией которого является дегрануляция тучных клеток и базофилов. [27,28] Образующиеся медиаторы вызывают повышение проницаемости стенок капилляров, активацию воспалительных клеток и разнообразные сердечно-легочные последствия анафилаксии. [27]
Анафилактический шок и угнетение функции миокарда
Рисунок 1 - Механизмы, лежащие в основе IgE-зависимого и IgE-независимого пути анафилаксии. ДВС = диссеминированное внутрисосудистое свертывание крови; ВВИГ = внутривенный иммуноглобулин; НПВП = нестероидные противовоспалительные препараты; PAF = фактор активации тромбоцитов; ФНО = фактор некроза опухоли.
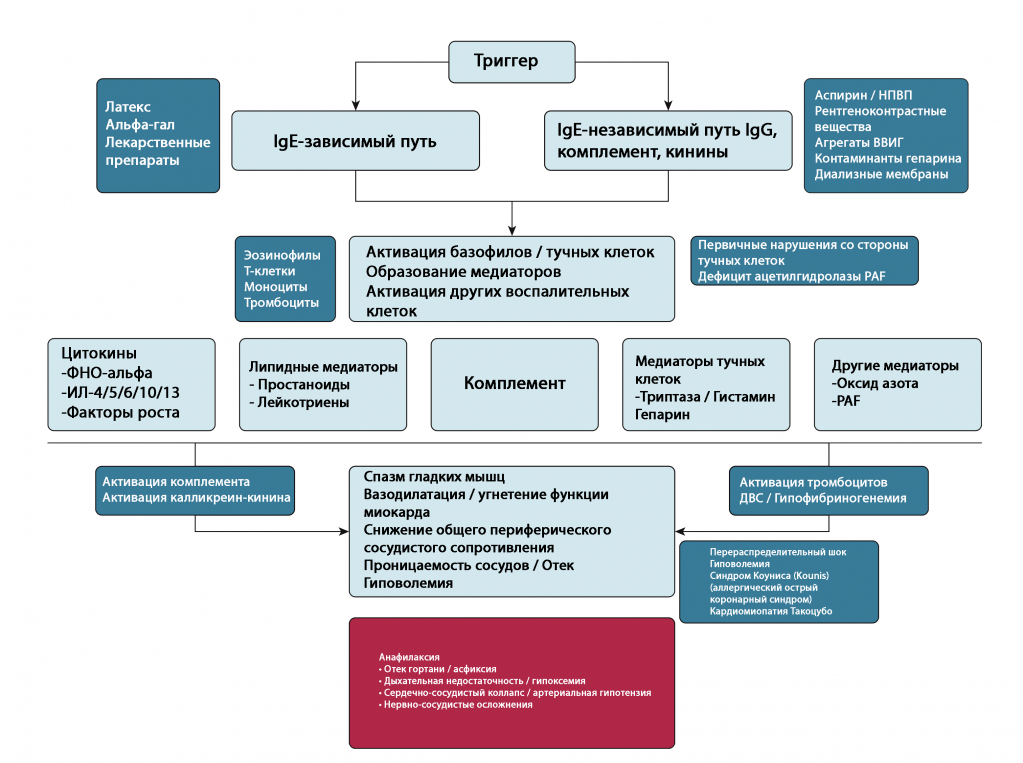
Анафилактический шок, рефрактерный к вазопрессорам, например, к адреналину, является редким, но опасным для жизни состоянием. Предположительно, он опосредован активацией гистамином путей передачи сигналов, которые приводят к образованию оксида азота в эндотелии. Оксид азота увеличивает синтез эндогенного вазодилататора, циклического гуанилатмонофосфата, за счет активации гуанилатциклазы. Исследования на животных показали, что этот процесс можно заблокировать внутривенным введением метиленового синего, который конкурентно ингибирует гуанилатциклазу и снижает образование циклического гуанилатмонофосфата. [35] Угнетение функции миокарда и артериальная гипотензия могут стать причиной гипоперфузии головного мозга и почек, причем первое осложнение приводит к обморокам и судорогам, а последнее - к почечной недостаточности.
Классификация и этиология анафилаксии
Иммунологические IgE-опосредованные реакции
|
Механизм |
Примеры |
Комментарии |
|
Иммунологический-IgE |
Пищевые аллергеныa |
8 распространенных пищевых аллергенов перечислены ниже |
|
(вторичное НАТК) |
Летучие аллергены |
Перхоть животных, аэрозолированные продукты питания, пыльца |
|
|
Латекс |
Перчатки, катетеры, маски, флаконы с лекарственными средствами |
|
|
Яд перепончатокрылых |
Медоносная пчела, оса, складчатокрылая оса, шершень, огненный муравей |
|
|
Лекарственная аллергия |
Антибиотики, биологические препараты,bвакцины, НПВПb |
|
|
Альфа-гал |
Мясо млекопитающих (говядина, свинина, оленина, баранина) |
|
|
ЗПАФН |
Физическая нагрузка + пища (пшеница, орехи, бобовые и т. д.) |
|
|
Гормоны |
Прогестерон или эстрогены (менструальные) |
|
|
Семенная жидкость |
Посткоитальная анафилаксия |
|
|
Рентгеноконтрастные средстваb |
Были зарегистрированы IgE-опосредованные реакции |
|
Иммунологический не-IgE |
Иммунные агрегаты |
Включает иммунные комплексы / комплемент |
|
|
ВВИГ |
Из антител IgG или IgE против IgA |
|
|
Аспирин и НПВПb |
Лейкотриен-управляемые и другие механизмы |
|
|
Диализные мембраны |
|
|
|
Рентгеноконтрастные средстваb |
Активация комплемента, генерация кининов |
|
|
Декстраны/ВМ железо |
|
|
|
Биологические препаратыb |
Ингибиторы цитокинов, омализумаб и др. |
|
|
Гепарин |
Генерация кининов контаминированным китайским гепарином |
|
Неиммунологический |
|
|
|
Прямые эффекты |
Опиаты, физические факторы |
Холод, жара, физическая нагрузка, солнечный свет |
|
Первичное НАТК |
МСАТК и системный |
Генетические дефекты влияют на пролиферацию или активацию тучных клеток |
|
САТКc |
|
Может быть связан с герминативными репликациями гена TPSAB1, кодирующего aльф-триптазу36 |
|
Идиопатический |
|
Повышенная чувствительность / дегрануляция тучных клеток |
|
|
|
Поляризация цитокина T-хелперов 2 |
|
|
|
Нераспознанные аллергены |
|
Маски |
Стридор Мюнхгаузена |
|
|
|
Недифференцированная соматоформная анафилаксия |
|
|
|
Дисфункция голосовых связок |
(a) Описаны как IgE-опосредованные, так и не-IgE-опосредованные реакции.
(b) Обычно молоко, яйца, пшеница, соя, орехи, арахис, моллюски и рыба.
(c) Нарушения со стороны тучных клеток связаны как с IgE-опосредованными аллергическими реакциями, так и со спонтанной дегрануляцией тучных клеток. [36]
Иммунологические не-IgE-опосредованные реакции
Неиммунологические анафилактические реакции
Неиммунологические триггеры анафилаксии включают физические факторы (например, физическую нагрузку, холод, жару) и ятрогенные вещества (включая рентгеноконтрастные средства и опиаты), которые способны стимулировать прямую дегрануляцию тучных клеток. [45,46] При первичных нарушениях со стороны тучных клеток тучные клетки могут дегранулировать как независимо, так и в ответ на аллергены, например, продукты питания и лекарственные препараты. [47]
Специфические синдромы и расстройства, связанные с анафилаксией
Недавно были описаны пациенты с тяжелыми нежелательными реакциями на олигосахарид альфа- галактозу, который есть в мясе млекопитающих и в химиотерапевтическом препарате цетуксимабе. Эти пациенты характеризуются развитием крапивницы или отсроченных анафилактических реакций на красное мясо и часто имеют в анамнезе укусы клещей. [37,49,50]
Согласно оценкам, от 30% до 60% пациентов, страдающих анафилаксией, могут не иметь явного этиологического фактора, объясняющего заболевание, и, следовательно, описываются как лица, имеющие идиопатическую анафилаксию (ИА) - диагноз исключения. [57-59] Последние достижения в патофизиологии очертили новые этиологические факторы, включая нарушения активации тучных клеток, синдромы гормоночувствительности (включая менструальную анафилаксию) и аллергию на альфа-галактозу.
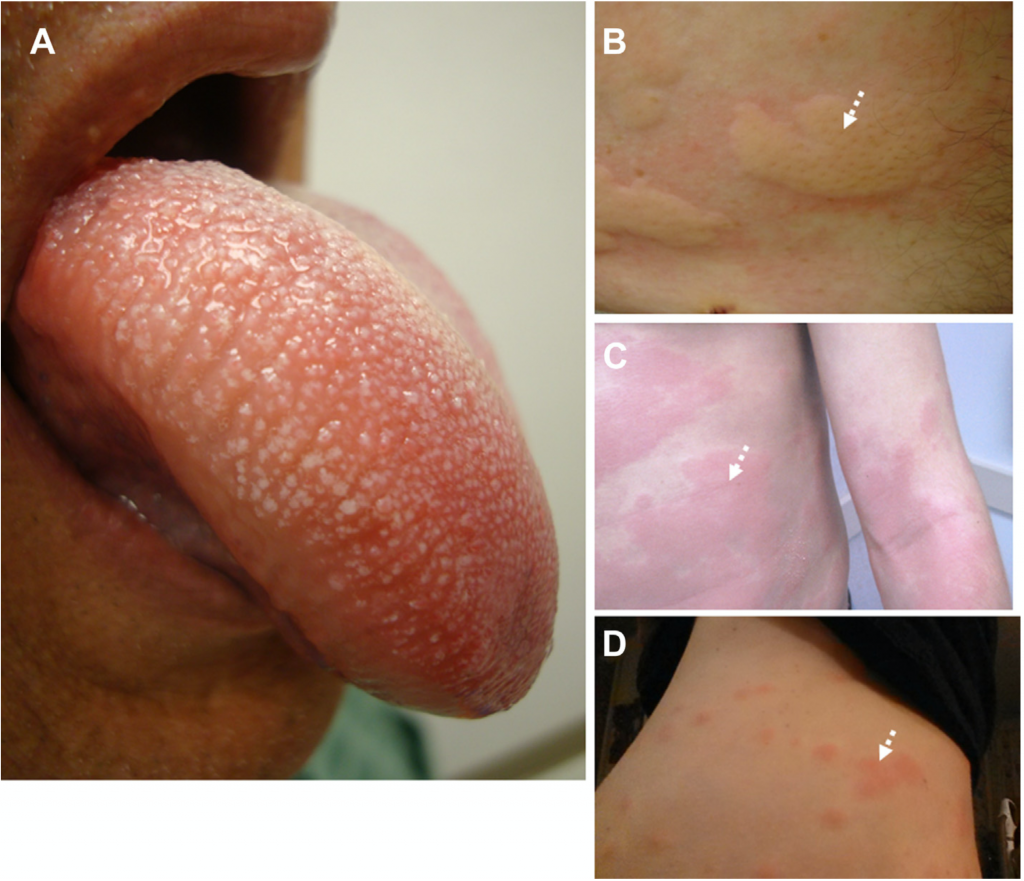
Клиническая картина анафилаксии
Таблица 3. Клинические признаки анафилаксии
|
Система органов |
Проявления |
Последствия |
|
Кожа / слизистые оболочки (80%-90%) |
Крапивница |
Гиповолемия |
|
|
Ангионевротический отек |
|
|
|
Ротоглотки |
Обструкция дыхательных путей |
|
|
Гортани |
Стридор |
|
|
|
Обструкция дыхательных путей |
|
|
Кишечника |
Боль в животе |
|
|
Приливы крови к лицу |
Артериальная гипотензия |
|
|
Зуд (ладони / подошвы / полость рта / половые органы) |
|
|
Бронхолегочная |
Отек гортани |
Охриплость / стридор |
|
(60%-70%) |
|
Дисфония |
|
|
Хрипы в легких/ кашель |
Дыхательная недостаточность |
|
|
|
Гипоксемия / цианоз |
|
|
Ринит |
Заложенность носа |
|
Сердечная |
Расширение сосудов / снижение ОПСС |
Артериальная гипотензия / шок |
|
(40%-50%) |
Вазоконстрикция в миокарде |
Снижение СВ |
|
|
Угнетение функции миокарда |
Ишемия миокарда |
|
|
|
Аритмия |
|
|
|
Остановка сердца |
|
Желудочно-кишечная |
Тошнота, рвота |
Обезвоживание |
|
(40%-50%) |
Диарея |
Гиповолемия |
|
|
Отек кишечника |
Боль в животе |
|
Неврологическая |
Головокружение |
обморок |
|
(<15%) |
Спутанность сознания |
Судороги |
|
|
Головная боль |
|
|
|
Чувство страха смерти |
|
|
|
Сужение полей зрения |
|
|
Мочеполовая |
Мышечные спазмы матки (♀) |
Боль |
|
|
Маточное кровотечение (♀) |
|
|
|
Отек мошонки (♂) |
Боль |
|
Разное |
Недержание мочи / кала |
|
| |
|
1. Возраст |
Мальчики в возрасте <15 лет и женщины в возрасте > 15 лет |
|
2. Путь введения аллергена |
Парентеральный > прием внутрь |
|
3. Прерывание приема лекарственных средств |
Пример: прерывание инсулинотерапии после десенсибилизации |
|
4. Наличие атопии в анамнезе |
Пример: анафилаксия на латекс, РКС, АФН и ИА |
|
5. Предшествующее воздействие |
Пример: использование протамин- цинк- инсулина (NPH) и реакция на протамин, применяемый для купирования действия гепарина |
|
6. Бронхиальная астма |
Более тяжелая бронхиальная астма увеличивает риск анафилаксии |
|
7. Географический регион |
Более высокая заболеваемость в северных широтах |
|
8. Пол |
Реакции на латекс, аспирин и некоторые лекарственные средства чаще встречаются у женщин. |
|
|
Реакции на яд животных чаще встречаются у мужчин. |
|
Факторы риска тяжелой анафилаксии |
|
|
1. Младенцы и пожилые люди |
|
|
2. Сопутствующие заболевания |
Астма, ишемическая дилатационная кардиомиопатия, ИБС |
|
3. Использование лекарственных средств |
Антигипертензивные препаратыа |
|
|
Ингибиторы моноаминоксидазы и трициклические антидепрессанты |
|
4. Нарушение когнитивных функций |
Алкоголь, седативные препараты, психоактивные вещества |
(a) Бета-адреноблокаторы, блокаторы кальциевых каналов, ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов ангиотензина, прямые ингибиторы ренина.
Дифференциальный диагноз
Диагностические исследования: триптаза и гистамин
Уровни гистамина в плазме крови повышаются через 5-10 минут после начала развития анафилаксии и также могут быть измерены. Однако концентрация гистамина в плазме крови увеличивается временно, возвращаясь к норме в течение 60 минут, что делает это биомаркер малопригодным для анализа, если пациента обследуют более чем через 1 час после появления симптомов. Метаболиты гистамина в суточной моче могут быть повышены в течение 24 часов после индексного события анафилаксии.
Vadas и соавторы [31] показали, что уровни гистамина и триптазы в сыворотке крови повышаются не всегда, даже у пациентов с тяжелыми проявлениями анафилаксии, включающими нарушения со стороны кожи, желудочно-кишечного тракта и дыхательной или сердечно-сосудистой системы. Кроме того, уровни триптазы в сыворотке крови не всегда повышаются во время вызванной пищевыми продуктами анафилаксии. [66] В результате ученые проявляют все больше интереса к идентификации альтернативных сывороточных биомаркеров, таких как фактор активации тромбоцитов или карбоксипептидаза A3, которые более точно подтверждают диагноз анафилаксии и коррелируют с ее тяжестью, но их клиническое использование еще не было разработано. [31]
Другие возможные диагностические тесты включают исследования, помогающие оценить состояния, которые имитируют анафилаксию (Таблица 5). [8] Если в анамнезе есть подозрение на IgE-опосредованную анафилаксию, то для выявления триггера назначают аллергическую пробу (сывороточную или кожную), которая часто требует направления к сертифицированному аллергологу-иммунологу. [38] Это обследование может быть выполнено немедленно в отделении интенсивной терапии или амбулаторно после выписки.
Таблица 5. Дифференциальная диагностика анафилаксии
|
Возможные исследования | |
|
1. Вазовагальные и вазодепрессорные реакции |
Клиническая картина/ ЭКГ / АД |
|
2. Синдром постуральной ортостатической тахикардии |
Пассивная ортостатическая проба (тилт-тест) |
|
3. Судороги |
ЭЭГ |
|
4. ОНМК |
КТ или МРТ головного мозга |
|
Сердечно-сосудистая система |
|
|
1. Кардиогенный шок |
ТТЭхоКГ или КПОС |
|
2. Геморрагический шок |
Клиническое кровотечение/ ОАКa |
|
3. Вазодилататорный / перераспределительный / эндотоксический шок |
Микробиологическое исследование |
|
4. Синдром повышенной проницаемости капилляров (гиповолемический шок) |
Парапротеинемия |
|
Эндокринная система / приливы крови к лицу |
|
|
1. Карциноид |
5-HIAA в моче |
|
2. Феохромоцитома |
Катехоламины в моче/сыворотке крови |
|
3. VIP-секретирующие опухоли |
Уровень VIP |
|
4. Медуллярный рак щитовидной железы |
Кальцитонин в сыворотке крови |
|
5. Менопауза (приливы, чувство жара) |
ЛГ, ФСГ, уровень эстрогена |
|
6. Гипогликемия |
Уровень сахара в крови |
|
Ятрогенные состояния/ лекарственные препараты |
|
|
1. Ванкомицин («синдром индейца») |
Анамнез/ клиническая картина |
|
2. Ниацин (приливы крови к лицу) |
Анамнез/ клиническая картина |
|
3. Общие анестетики (артериальная гипотензия) |
Анамнез/ клиническая картина |
|
Токсические |
|
|
1. «Синдромы ресторана» |
|
|
a. Гистаминовое отравление |
Анамнез /триптаза/ гистамин |
|
b. ГН |
Токсикология |
|
2. Алкоголь |
Уровень EtOH / осмолярный разрывb |
|
3. Сульфиты |
Клиническая картина /токсикология |
|
Гематологические / злокачественные новообразованияc |
|
|
1. Системный мастоцитоз |
Триптаза, костный мозг |
|
2. Крапивница пигментная |
Биопсия кожи, триптаза |
|
3. Базофильный лейкоз |
Костный мозг |
|
4. Острый промиелоцитарный лейкоз с лечением третиноином |
Костный мозг |
|
Иммунологические |
|
|
1. Брадикинин-опосредованный ангионевротический отек |
Уровни ингибитора C4, C1 |
|
Инфекция |
|
|
1. Эхинококковая киста (Echinococcus granulosus) |
Клиническая картина, серология, рентгенологические исследования |
|
2. Сепсис / септический шок |
Микробиологическое исследование крови |
|
Психосоматические / функциональные расстройства |
|
|
1. Паническая атака |
Консультация психиатра |
|
2. Искусственная анафилаксия |
|
|
а. Стридор Мюнхгаузена |
Консультация психиатра |
|
3. Недифференцированная соматоформная анафилаксия |
Консультация психиатра |
|
4. Дисфункция голосовых связок |
Спирометрия/ петля «поток-объём» |
(a) Может быть в норме при острой потере цельной крови.
(b) Осмолярный разрыв позволяет проводить оценку других токсичных спиртов.
(с) Клональные и злокачественные заболевания тучных клеток часто характеризуются мутациями рецептора фактора стволовых клеток, c-kit.
Лечение
2. Критическое значение имеет удаление потенциального антигена-триггера, размещение пациента в положении лежа на спине и быстрое обеспечение проходимости дыхательных путей, поддержки дыхания и кровообращения. Положение пациента с анафилаксией может иметь важное значение. При анафилаксии преобладают вазодилатация и гиповолемия. Таким образом, пациенты чрезвычайно чувствительны к смещению объема жидкости, и внезапные изменения положения могут привести к остановке сердца с летальным исходом. [76] Несмотря на отсутствие проспективных данных, существует единодушное мнение о том, что пациенты должны находиться в положении лежа на спине, если это не противопоказано вследствие активной рвоты, дыхательной недостаточности или беременности; в этом случае более подходит положение лёжа на левом боку. [3,8,76,77] Возвышенное положение ног (или положение Тренделенбурга с использованием поворотного стола) остается спорным аспектом. Это положение может изначально помочь, когда пациенту проводят жизненно необходимую инфузионную терапию в отсутствие вазопрессоров. [78] Важно отметить, что это положение редко используется в отделении интенсивной терапии (кроме как во время процедур), так как вазопрессоры и внутривенные жидкости более эффективны и легко доступны. [8]
3. При дыхательной недостаточности пациент должен находиться в удобном положении, а стесняющую одежду следует снять или расстегнуть. Бронходилататор - короткодействующий β2 -агонист (альбутерол) - назначают в дозе 2,5 или 5 мг в 3 мл в виде раствора для небулайзера или два вдоха через дозированный аэрозольный ингалятор каждые 2-4 часа, пока не будет достигнуто симптоматическое облегчение или пациент не будет переведен в специализированное учреждение.
4. Необходимо обеспечить внутривенный доступ с использованием катетеров большого диаметра и как можно быстрее проводить инфузионную терапию. Допустимой альтернативой является внутрикостный (в/к) доступ.
Дополнительные методы лечения
Таблица 6. Общие подходы к лечению системной анафилаксии
|
Первоначальное лечение (в кабинете врача/ отделении неотложной терапии /больнице) |
Уровень доказательности |
|
Диагноз основан на клинической оценке |
C |
|
Рекомендуется раннее вмешательство |
|
|
Оценить риск серьезных / смертельных реакций (см. Таблицу 7) |
C |
|
Немедленные общие мероприятия (первая линия терапии) |
|
|
Разместить пациента в положении лежа на спине |
C |
|
Удалить потенциальный антиген-триггер |
C |
|
Обеспечить проходимость дыхательных путей, поддержку дыхания и кровообращения |
C |
|
Введение адреналина (переднебоковая часть ЛШМ, в/м) |
B |
|
(1 мл/кг 1:1000 адреналина или 0,3-0,5 мг) |
|
|
1. Повторить до 3 инъекций каждые 5-15 минут |
|
|
2. Если адреналин в/м неэффективен, обеспечьте мониторинг и попробуйте адреналин в/в |
C |
|
3. Если в/в доступ затруднен, обеспечьте в/к доступ и введите адреналин |
D |
|
Обеспечение проходимости дыхательных путей |
C |
|
Кислород (до 100% через маску) |
D |
|
Ввести альбутерол через небулайзер для лечения бронхоспазма |
B |
|
Подготовьтесь к интубации при наличии стридора или нарушения проходимости дыхательных путей |
|
|
Быстро вводите в/в жидкости / кристаллоиды |
B |
|
30 мл/кг через катетеры большого диаметра в первый час для лечения артериальной гипотензии; если объем циркулирующей жидкости увеличивается, продолжайте инфузионную терапию |
|
|
Дополнительные методы лечения (после введения адреналина) |
|
|
Введите H1 антигистаминный препарата |
B |
|
Введите H2 антигистаминный препаратb |
B |
|
Введите кортикостероиды |
|
|
Метилпреднизолон (1-2 мг/кг) в/в |
B |
|
Дополнительные мероприятия (в больнице/ отделении интенсивной терапии) |
|
|
Рефрактерная артериальная гипотензия |
|
|
После бета-блокады |
|
|
Глюкагон (3-10 мг в/в медленно у взрослых) с последующей
|
B |
|
| |
|
После нескольких доз адреналина внутримышечно |
|
|
Непрерывная в/в инфузия адреналина |
C |
|
(Смешайте 1 мл адреналина 1: 1000 с 1000 мл 5% декстрозы или 0,9 физиологического раствора; инфузия со скоростью 5-15 мкг/мин, максимально 10 мкг/мин) |
|
|
Болюсное введение адреналина: при угрожающем сердечно-сосудистом коллапсе (50 мкг / 0,5 мл 1: 10000 медленно внутривенно струйно) |
|
|
Рассмотрите другие вазопрессоры, в том числе допамин или вазопрессин |
|
|
Асфиксия / нарушение дыхания / остановка дыхания |
|
|
Оксигенация |
|
|
Оценка степени отека дыхательных путей |
|
|
Адреналин через небулайзер / рацемический адреналин (0,5 мл, 2,25% каждые 20 минут для лечения стридора) |
|
|
Интубация / постинтубационное управление искусственной вентиляцией легких |
C |
|
Избегайте лекарственных средств, которые снижают АД |
|
|
Избегайте применения миорелаксантов для интубации, если это возможно |
|
|
Рекомендуется фиброоптическая интубация при сохранном уровне сознания пациента, если это возможно |
|
|
(если есть подозрение на поражение гортани) |
|
|
Седатировать и дождаться адекватного времени выдоха |
|
|
Минимизировать задержку дыхания и баротравму |
|
|
Использование кетамина связано с бронходилатацией |
|
|
(с осторожностью рекомендуется применять кетамин у пациентов с сердечно-сосудистыми заболеваниями) |
|
|
При нарушении проходимости дыхательных путей рассмотреть крикотиреоидотомию |
|
|
Экстракорпоральная мембранная оксигенация |
D |
|
Рассмотреть при недостаточном эффекте |
|
|
Рассмотреть на раннем этапе и часто в случаях, когда пациент имеет ограниченную чувствительность к вазопрессорам |
|
|
Ведение пациента после выписки |
|
|
Обучение |
|
|
Определение и избегание триггеров |
|
|
План действий при анафилаксии |
|
|
Назначение автоинжектора адреналина |
Классы рекомендаций основаны на уровнях доказательности: A = рандомизированные исследования; B = контролируемое исследование без рандомизации; C = исследование типа «случай-контроль», сравнительные или корреляционные исследования; D = мнение / отчеты экспертов или основано на опыте органов власти): сильная рекомендация (класс А), умеренная рекомендация (классы В и С) и слабая рекомендация (класс D). С изменениями по: Campbell RL и соавт.3 переднебоковая часть ЛШМ = переднебоковая часть латеральной широкой мышцы бедра; в/к = внутрикостный.
(a) Например, дифенгидрамин 1-2 мг/кг.
(b) Например, ранитидин 1-2 мг/кг.
Дополнительные мероприятия (в больнице/ отделении интенсивной терапии)
Лечение дыхательных осложнений: асфиксия / дыхательная недостаточность
Можно вводить рацемический адреналин с помощью небулайзера для уменьшения отека гортани и для облегчения интубации. В некоторых сообщениях адреналин вводили эндотрахеально или сублингвально, если происходила задержка в получении внутривенного доступа. [3] Во время интубации и искусственной вентиляции легких следует стараться избегать использования седативных препаратов или лекарственных препаратов, снижающих АД. Минимизация задержки дыхания и избегание баротравмы также необходимы для предотвращения дальнейшего ухудшения состояния. Использование кетамина при анафилаксии было связано с бронходилатацией.
Рефрактерная артериальная гипотензия
Таблица 7. Лекарственные средства, используемые при лечении анафилаксии
|
Эффектылекарственного средства |
Концентрация |
Доза |
Путь введения |
Кратность введения |
Нежелательные эффекты |
|
Адреналин |
1:1,000 (1 мг/мл) |
0,01 мг/кг 0,3 - 0,5 мг |
в/м |
Каждые 5-15 минут |
Тахикардия, учащенное сердцебиение, тахиаритмии, тревога, учащенное сердцебиение, приливы крови к лицу |
|
|
1:10000 (0,1 мг/мл) |
0,01 мг/кг 0,5-1,0 мг (5-10 мл) |
в/в |
Каждые 5-15 минут Струйно |
См. выше |
|
Вазопрессин |
NA |
0,04 Ед |
в/в |
В минуту |
Ишемия |
|
Дофамин |
NA |
1-50 мкг/кг |
в/в |
В минуту |
Тахикардия, тахиаритмии |
|
Норадреналин |
NA |
0,02-1 мкг/кг |
в/в |
В минуту |
Тахикардия, тахиаритмии |
|
Альбутерол |
|
|
|
|
|
|
ДАИ |
2,5 мг в одном вдохе |
1-2 вдоха (2,5-5 мг) |
ИНГ |
Каждые 2-4 ч |
Тахикардия, учащенное сердцебиение, тревога |
|
Через небулайзер |
2,5 мг/3 мл |
3 мл |
ИНГ |
Каждые 2-4 ч |
См. выше |
|
|
5 мг/3 мл |
3 мл |
ИНГ |
Непрерывно |
См. выше |
|
Глюкагон |
|
3-10 мгa 0,05-0,1 мг/кг/ч |
в/в в/в |
Однократно Непрерывно |
Тошнота, рвота, тахикардия |
|
Дифенгидрамин |
|
|
|
|
|
|
Лечение |
NA |
25-50 мг |
в/в, п/оb |
Однократно |
Сонливость, седация |
|
Профилактика |
NA |
25-50 мг |
|
Однократно c |
|
|
Кортикостероиды |
|
|
|
|
|
|
Гидрокортизон |
NA |
100 мг |
в/в |
Каждые 8 ч |
Гипергликемия |
|
Преднизонd |
|
|
|
|
|
|
Лечение |
NA |
1-2 мг/кг |
п/оb |
Однократно |
Возбуждение, тревога, психоз |
|
Профилактика |
NA |
50 мг |
п/оb |
За 13 ч, затем за 7 ч, затем за 1 ч |
См. выше |
(a) Медленная инфузия в течение 2-5 минут, чтобы свести к минимуму тошноту и рвоту.
(b) Избегайте применения пероральных лекарственных препаратов у пациентов с тошнотой, рвотой или невозможностью защитить дыхательные пути (если нет интубации и желудочного зонда).
(с) За 1 ч до процедуры.
dв/в альтернативы следует дозировать в расчете на эквиваленты преднизона.
Рисунок 3 - Примеры лекарственных препаратов, обычно используемых при лечении анафилаксии (любезно предоставлено Майклом Кинсом, PharmD и Джонни Перри, RPh, Медицинский центр Поминовения Крестителя (Michael Keens, PharmD, Johnny Perry, RPh, Wake Baptist Medical Center)). А, Адреналин 1 мг/мл (1: 1000). B, Автоинжектор ЭпиПен 0,3 мг. C, Правильное место для самостоятельной в/м инъекции в середине наружной поверхности бедра (переднебоковая часть латеральной широкой мышцы бедра, середина мышечного брюшка). D, Вазопрессин 20 Ед/мл. Е, Дифенгидрамин 50 мг/мл. F, Фамотидин 20 мг в 50 мл. G, Метиленовый синий, концентрация 1 мг/мл. H, Метилпреднизолон, флакон 1 г.
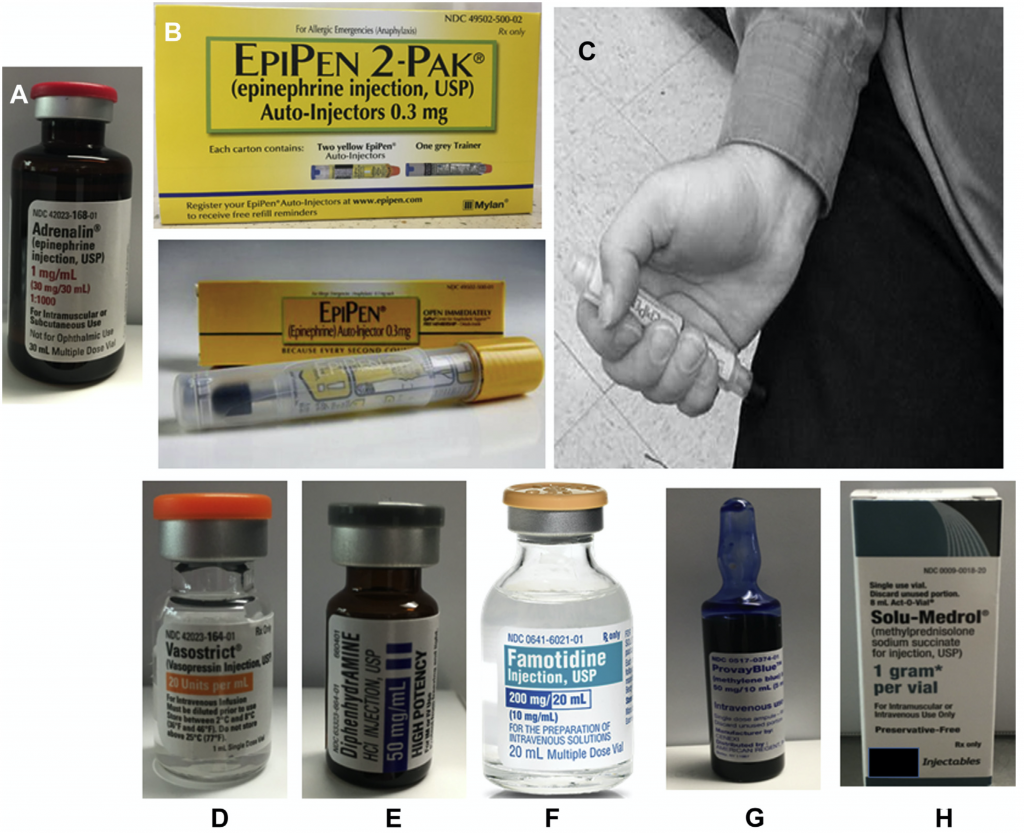
В редких случаях, когда происходит быстрое ухудшение состояния, адреналин можно вводить с помощью болюсной инъекции (от 0,5 до 1,0 мг или от 5 до 10 мл в разведении 1: 10000 с помощью медленного в/в или в/к струйного введения) или 1 мл в разведении 1: 10000 с помощью в/в или в/к болюсного введения в случае угрожающей или наступившей остановки сердца. Нежелательные эффекты адреналина включают тревогу, приливы крови к лицу, тахикардию, предсердную или желудочковую аритмию, нарушение мозгового кровообращения и артериальную гипертензию. Могут быть доступны специальные лекарственные формы для немногочисленных пациентов с аллергией на сульфиты. Иногда у пациентов можно добиться эффекта от дополнительной инфузии вазопрессора помимо адреналина при рефрактерном анафилактическом шоке. Вазопрессин и/или фенилэфрин могут использоваться для повышения общего периферического сосудистого сопротивления, не вызывая чрезмерной тахикардии. Если у пациента относительная брадикардия, то можно добавить норадреналин или допамин. Был опубликован примечательный успешный случай лечения рефрактерной анафилаксии с помощью метиленового синего, в котором была описана синергия с адреналином; следует учитывать, однако, что в редких случаях метиленовый синий сам по себе способен вызывать анафилаксию. [35,82]